با توجه به اینکه نانوذرات آلی دارای تعداد زیادی گروه عملکردی هستند که باعث میشود به بهترین شکل ممکن به داروها و فاکتورهای رشد (GFها) متصل شوند و همچنین یونهایی که توسط نانوذرات فلزی آورده میشوند دارای خواص ضد باکتریایی موثری هستند، این نانوذرات پتانسیل بالایی در درمان زخمهای دیابتی نشان میدهند.
با پیشرفت روزافزون جامعه و تکنولوژی، محققان نانوذرات با خواص بیولوژیکی متعددی را کشف کردهاند که میتوانند در درمان زخمهای دیابتی بهبود موثری ایجاد کنند و برخی از نقاط ضعف مربوط به درمانهای بالینی را اصلاح نمایند.
در مقاله پیشین به معرفی زخمهای دیابتی پرداختیم در این مقاله، به بررسی کاربردهای اخیر نانوذرات آلی، از جمله نانوذرات پلیمری و اگزوزومها، و همچنین نانوذرات معدنی، شامل فلزها و نانوذرات غیرفلزی و غیره، در درمان و ترمیم زخمهای دیابتی میپردازد، که در شکل ۱ به طور خلاصه نمایش داده شده است.

شکل ۱: تصویر شماتیک طبقهبندی و مکانیسم درمانی بیومواد مورد استفاده در زخمهای دیابتی. مواد زیستی با مولکولهای آلی (شامل پروتئین بارگذاری شده، اگزوزومها و ترکیبات مولکولی کوچک و غیره) و مولکولهای معدنی (شامل AgNPs، CeNPs، SiO2NP و غیره) بارگذاری میشوند تا زخم دیابتی را بهبود بخشند.
نانوذرات آلی در ترمیم زخمهای دیابتی
نانوذرات حاوی پروتئین میتوانند فاکتورهای رشد مختلفی را آزاد کنند و به عنوان حاملهایی عمل میکنند که پایداری و کنترل آزادسازی این فاکتورها در نواحی زخم را بهبود میبخشند، به ویژه در زخمهای دیابتی که کمبود فاکتورهای رشد دارند و در نتیجه، ترمیم بافت مشکل است. استفاده از EGF در درمان زخمهای دیابتی رایج است اما به دلیل نیمه عمر کوتاه آن، نیاز به رویکردهای جدیدی برای تثبیت و افزایش ماندگاری آن وجود دارد.
توسعه نانوذرات مبتنی بر پلیمرهایی مانند پلی لاکتیک اسید/اسید گلیکولیک و الاستین-لایک پپتایدها (ELPs) اجازه میدهد تا فاکتورهای رشد مانند EGF و VEGF با ثبات بیشتر و بدون از دست دادن فعالیت بیولوژیکیشان آزاد شوند. این نانوذرات نه تنها فعالیت بیولوژیکی فاکتورهای رشد را حفظ میکنند بلکه به تحریک تکثیر فیبروبلاستها و بهبود آنژیوژنز نیز کمک میکنند که نهایتاً منجر به بهبود زخمهای دیابتی و غیردیابتی میشود. همچنین، آنها میتوانند چندین فاکتور رشد را به طور همزمان ارائه دهند که پتانسیل بازسازی کامل لایههای پوست را فراهم میآورد.
برای به حداکثر رساندن کارایی درمانی، تحقیقات به سمت توسعه سیستمهای دارورسانی پیشرفتهتری میروند که میتوانند فاکتورهای رشد را به طور موثرتر و با ثبات بیشتری تحویل دهند.
اگزوزوم: اگزوزومهای مشتق از سلولهای بنیادی مزانشیمی مغز استخوان نسبت به فیبروبلاستها سطوح بالاتری از کلاژن، FGF، و VEGF تولید میکنند و در نتیجه، باعث افزایش سرعت رگزایی میشوند. به منظور حفظ عملکرد و آزادسازی پایدار اگزوزومها برای التیام زخم، توسعه داربستهای زیست سازگار اهمیت دارد.
وانگ و همکاران داربست اتیلن پروپیلن فلوئوردار مبتنی بر پلیساکارید را تهیه کردند که خواص منحصر به فردی مانند خودترمیمی، قابلیت تزریق، چسبندگی، ضد میکروبی بودن، خاصیت هموستاتیک، و مقاومت در برابر اشعه UV دارد.
این خواص از طریق استفاده از آمینه پلیاتیلن و آلدئید پلیاولان توسط واکنش پایه شیف برگشت پذیر به دست آمدهاند. این داربستها قابلیت بارگیری اگزوزومها و آزادسازی مداوم آنها را با حفظ فعالیت بیولوژیکی دارند که میتواند به تکثیر، مهاجرت، و تشکیل لولههای سلولهای اندوتلیال کمک کند، در نهایت رگزایی و بهبود زخمهای دیابتی را تسریع بخشد. این تحقیق نشان میدهد که اگزوزومها، به علت ساختار منحصر به فرد خود، میتوانند بارگیری و اندوسیتوز را به طور موثرتری انجام دهند و در فرآیند بهبود زخم با تقویت تکثیر و مهاجرت فیبروبلاستها نقش داشته باشند.
بهینهسازی یک هیدروژل متیلسلولز-کیتوزان بارگذاری شده با اگزوزوم به عنوان گزینهای ترمیمی نشان داده شده است که میتواند به بازیابی ساختاری و عملکردی زخم در مدلهای دیابتی کمک کند. اگزوزومها به دلیل عملکرد بالا، زیست فعالی، و زیست سازگاریشان، پتانسیل زیادی در بهبود زخمهای دیابتی و سایر زخمهای عروقی دارند.
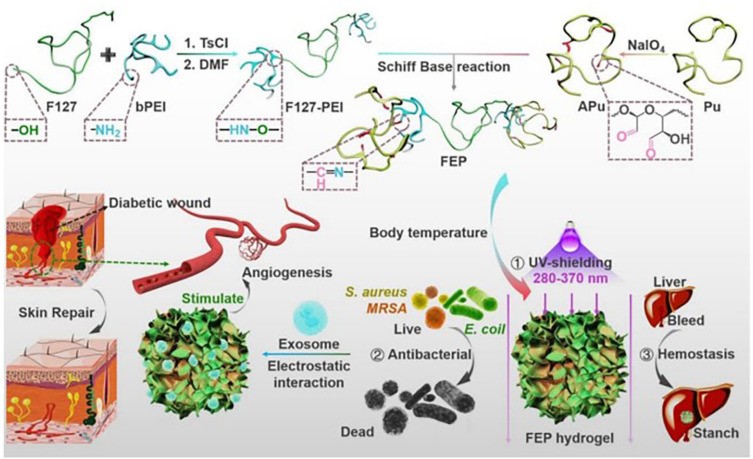
شکل ۲: تصویر شماتیک سنتز F127-PEI، APu، پانسمان داربست چند منظوره FEP، پانسمان داربست FEP حاوی اگزوزوم در مقیاس نانو و کاربرد بالقوه در ترمیم زخم دیابتی و بازسازی پوست را نشان می دهد.
نانوذرات حاوی اسید نوکلئیک: نانوذرات حاوی اسید نوکلئیک میتوانند در درمان زخمهای دیابتی مزمن و غیرقابل ترمیم موثر باشند، زیرا این نانوذرات قادر به بیان سیتوکینها و فاکتورهای رشد (GF) هستند که نقش حیاتی در ترمیم زخم دارند. استفاده از پلاسمیدهایی که ژنهای مربوط به این فرآیندها را بیان میکنند، نشان دادهاند که بهبود قابل توجهی در زخمهای دیابتی ایجاد میکنند.
ترکیب پلاسمیدی که ژنهای VEGF-A و PDGF-B را همزمان بیان میکند با نانوکرههای PLGA، به ترمیم زخمهای دیابتی کمک کرده و باعث تنظیم مثبت بیان این ژنها شده است. علاوه بر این، نانوذرات میتوانند به کاهش بیان غیرطبیعی MMP-9 در محل زخم کمک کنند و با استفاده از پانسمانهای حاوی siRNA، بیان این پروتئین را در زخمهای دیابتی کاهش دهند که به تسریع در فرآیند ترمیم زخم کمک میکند.
این فناوریها همچنین با تعدیل مسیرهای سیگنالینگ و ژنهای مرتبط، ترمیم زخم را بهبود میبخشند و میتوانند فرآیند آنژیوژنز را افزایش دهند. به طور کلی، نانوذرات حاوی اسید نوکلئیک، ابزارهای قدرتمندی برای درمان زخمهای دیابتی ارائه میدهند که از طریق تنظیم کنترل شده عوامل بیولوژیکی و ژنتیکی عمل میکنند.
نانوذرات حاوی نیتریک اکسید: نانوذرات حاوی نیتریک اکسید (NO) دارای عملکردهای بیولوژیکی قابل توجهی هستند، از جمله خواص ضد باکتریایی قوی، توانایی در مقابله با بیوفیلمها و ترمیم زخم. NO میتواند عروق خونی را گشاد کند، به عنوان یک مولکول سیگنالدهنده عمل کند و چرخه پیامرسانی درون سلولی گلوکز مونو فسفات (GMP) را تنظیم مینماید.
علاوه بر این، با آسیب رساندن به DNA باکتریها و مختل کردن دیواره سلولی آنها، باعث از بین رفتن باکتریهای مقاوم مانند MRSA میشود. با توجه به نیمه عمر کوتاه و محدوده انتشار کوچک NO، برای رساندن موثر NO به ناحیه زخم، استفاده از سیستمهای تحویل مانند S-nitrosoglutathione (GSNO، یک دهنده درون زا NO) در نانوذرات PLGA ضروری است.
نانوذرات بارگذاری شده با ترکیب مولکولی کوچک: مطالعات نشان دادهاند که نانوذرات بارگذاری شده با ترکیبات مولکولی کوچک مانند کورکومین (Cur)، که دارای خواص ضدالتهابی، آنتی اکسیدانی، ضدباکتریایی و ضدتوموری است، میتوانند در درمان زخمهای دیابتی موثر باشند. با این حال، به دلیل فراهمی زیستی کم و پایداری ضعیف کورکومین، استفاده از آن دشوار است.
نانوذرات کیتوزان سولفاتی آراسته به کورکومین (Cur-CS-NPs) تولید شدهاند که پایداری و حلالیت کورکومین را بهبود میبخشند و نتایج مثبتی در مدلهای دیابتی نشان دادهاند. این نانوذرات نه تنها التهاب ناشی از ماکروفاژها را کاهش میدهند، بلکه آنژیوژنز را نیز افزایش میدهند و بهبود زخم را تسریع میکنند.
استفاده از این نانوذرات در هیدروژلها (Cur-NP/HG) باعث افزایش سرعت بهبود زخمهای پوستی دیابتی شده و به بهبود قابل توجهی در تولید بافت گرانوله و رسوب کلاژن منجر میشود. در مجموع، این تکنولوژیها با استفاده از حاملهای نانویی مناسب، به حداکثر رساندن اثربخشی درمانی ترکیبات مولکولی کوچک را امکانپذیر میسازند و به طور قابل توجهی در درمان زخمهای دیابتی موثر هستند.
علاوه بر این، برخی از این ترکیبات از گیاهان استخراج میشوند. به عنوان مثال، اسید فرولیک (FA) قبلاً گزارش شده است که دارای خواص دوگانه ضد دیابتی و آنتی اکسیدانی است. نانوذرات FA با استفاده از روش نانو رسوب تهیه شدند و اثرات هیپوگلیسمی و ترمیم زخم آنها مورد ارزیابی قرار گرفت. با این حال، یک اثر ضد باکتریایی ناپایدار را نشان میدهد. بنابراین، روزمن و همکاران از CS به عنوان یک ماده کپسولهکننده برای حفظ فعالیت ضد میکروبی آن استفاده کردند.
علاوه بر این نانوذرات، از نانوذرات ترکیبی مصنوعی نیز استفاده میشود. تحت القای فاکتور القاکننده هیپوکسی (HIF-1α) ، VEGF، SDF-1 و هم اکسیژناز-1 (HO-1) با سرعت بیشتری سنتز میشوند.
زخمهای دیابتی به دلیل سطوح پایینتر HIF-1α، بیان VEGF و SDF-1α را کاهش دادهاند و علاوه بر این، محیط هایپرگلیسمی که در محل زخم ROS بیشتری تولید میکند، باعث تغییر HIF-1α coactivator p300 میشود و سبب کاهش فعال سازی ترانس با واسطه HIF-1α، در ژن های هدف می شود. هر دوی این موارد بهبود زخم در بیماران دیابتی را دشوار میکند.
دسفری اکسامین (دسفرال) با تضاد رقابتی پرولین هیدروکسیلاز (PHD) و شلاته کردن آهن از ناحیه زخم از هیدروکسیلاسیون HIF-1α و تخریب پروتئازومی بعدی آن جلوگیری میکند که متعاقباً باعث افزایش رگزایی، کاهش التهاب و بلوغ زخم میشود.
تهیه و تنظیم از:
- سویل راجی
- مهسا سبزی خباز