تصور کنید که درباره آخرین پروژه علمی خود به دوستانتان میگویید: استفاده از یک باتری برای روشن کردن یک لامپ.
ممکن است با نگاههای خیره مواجه شوید… کمی خستهکننده و ساده به نظر میرسد، درست است؟ حالا به آنها بگویید که میخواهید این کار را با یک سیب زمینی انجام دهید! بله، شما واقعاً میتوانید از میوهها و سبزیجات به عنوان بخشی از منبع تغذیه الکتریکی استفاده کنید!
باتریها انرژی وسایل زیادی را در اطراف شما تامین میکنند، از جمله تلفنهای همراه، دستههای بازی بیسیم، و آشکارگر (detector) دود. در این پروژه علمی، شما با مبانی علم باتری آشنا خواهید شد و از سیب زمینی برای ساختن یک باتری ساده برای تامین انرژی یک چراغ کوچک و یک زنگ استفاده میکنید.
هدف
اندازهگیری تغییرات ولتاژ و جریان باتریهای سیب زمینی هنگامی که آنها را به صورت سری یا موازی در مدار میبندید.
مقدمه
باتریها مخازنی هستند که انرژی را ذخیره میکنند، و میتوان از آنها برای تولید برق استفاده کرد. این روش ذخیرهسازی انرژی به ما امکان میدهد تا دستگاههای الکترونیکی قابل حمل بسازیم (تصور کنید چه دردسری خواهد بود اگر همه چیز لازم باشد به پریز دیواری وصل شود تا کار کند!). انواع مختلفی از باتری ها وجود دارد، اما همه آنها برای تولید برق به نوعی واکنش شیمیایی وابسته هستند.
واکنش شیمیایی معمولاً بین دو قطعه فلز، به نام الکترودها، و یک مایع یا خمیر، به نام الکترولیت رخ میدهد. اتفاقاً رطوبت داخل سیب زمینی به خوبی به عنوان الکترولیت کار میکند، پس فقط نیاز است که چند الکترود فلزی به سیب زمینی اضافه کنید و شما یک باتری خواهید داشت! اگرچه نیازی نیست جزئیات واکنش شیمیایی را برای انجام این پروژه بدانید، اما در ادامه یکسری توضیحات داده شده است.
در مرحله بعد، شما باید برخی مفاهیم اساسی در مورد برق را بدانید.
جریان برق به نام جریان الکتریکی شناخته میشود که با واحدی به نام آمپر (A) (همچنین به اختصار آمپ گفته میشود) اندازهگیری میشود.
ولتاژ، که با ولت (V) اندازهگیری میشود، نیرویی است که جریان الکتریکی را از طریق سیمها عبور میدهد.
در نهایت، مقاومت الکتریکی که با اهم (Ω) (حرف بزرگ یونانی امگا) اندازهگیری میشود، معیاری برای سختی جریان برق از طریق یک ماده خاص است.
یک قیاس رایج برای الکتریسیته این است که تصور کنید آب در یک لوله جریان دارد. مقدار آب جاری مانند جریان است. فشاری که آب را هل میدهد مانند ولتاژ است. مقاومت مانند اندازه لوله است—اینکه مقدار زیادی آب را به سرعت از یک لوله بسیار کوچک نسبت به یک لوله بزرگ عبور دهید، سختتر است. آیا به نظر می رسد که چیزهای زیادی برای یادآوری وجود دارد؟ جدول ۱ ولتاژ، جریان و مقاومت را خلاصه میکند.
جدول ۱. خلاصهای از اصطلاحات پایه الکتریکی.
| کمیت | واحد | توضیحات |
|---|---|---|
| جریان | آمپر (A) | جریان الکتریسیته |
| ولتاژ | ولت (V) | فشاری که باعث جریان برق میشود |
| مقاومت | اهم (Ω) | سختی عبور جریان الکتریسیته از یک جسم |
یک مدار الکتریکی مسیری است که از طریق آن برق میتواند جریان یابد. مدارها میتوانند بسیار پیچیده باشند، با میلیونها و میلیونها جزء (مانند آنهایی که درون کامپیوتر شما هستند)، یا بسیار ساده، با فقط دو جزء، مانند یک باتری و یک لامپ.
این پروژه بر روی مدارهای ساده متکی به باتری تمرکز خواهد کرد. به طور کلی، یک باتری ولتاژ معینی را به مدار میرساند. اینکه چه مقدار جریان از باتری خارج می شود به بار یا آنچه باتری به آن متصل است بستگی دارد.
باتریها دارای پایانههای مثبت و منفی هستند. برای اینکه الکتریسیته در مداری که با باتری کار میکند جریان یابد، باید یک مسیر کامل از پایانه مثبت، از طریق بار و بازگشت به پایانه منفی وجود داشته باشد. به این مدار بسته می گویند. اگر مسیر قطع شود (برای مثال، اگر یک سیم قطع شود)، برق نمیتواند جریان یابد. به این مدار باز میگویند.
در نهایت، اگر مسیر مستقیمی از پایانه مثبت به پایانه منفی وجود داشته باشد، به آن اتصال کوتاه میگویند. اتصال کوتاه بد است زیرا میتوانند باعث تخلیه سریع باتریها و داغ شدن آنها شوند (خوشبختانه، باتریهای سیب زمینی فقط میتوانند مقدار کمی جریان تأمین کنند، بنابراین اتصال کوتاه در این آزمایش خطرناک نیست).
تصویر ۱ نمودارهای مدار باز، بسته و اتصال کوتاه را نشان میدهد.
یک مدار الکتریکی مسیری است که از طریق آن برق میتواند جریان یابد. مدارها میتوانند بسیار پیچیده باشند، با میلیونها و میلیونها جزء (مانند آنهایی که درون کامپیوتر شما هستند)، یا بسیار ساده، با فقط دو جزء، مانند یک باتری و یک لامپ.
این پروژه بر روی مدارهای ساده متکی به باتری تمرکز خواهد کرد. به طور کلی، یک باتری ولتاژ معینی را به مدار میرساند. اینکه چه مقدار جریان از باتری خارج می شود به بار یا آنچه باتری به آن متصل است بستگی دارد.
باتریها دارای پایانههای مثبت و منفی هستند. برای اینکه الکتریسیته در مداری که با باتری کار میکند جریان یابد، باید یک مسیر کامل از پایانه مثبت، از طریق بار و بازگشت به پایانه منفی وجود داشته باشد. به این مدار بسته می گویند. اگر مسیر قطع شود (برای مثال، اگر یک سیم قطع شود)، برق نمیتواند جریان یابد. به این مدار باز میگویند.
در نهایت، اگر مسیر مستقیمی از پایانه مثبت به پایانه منفی وجود داشته باشد، به آن اتصال کوتاه میگویند. اتصال کوتاه بد است زیرا میتوانند باعث تخلیه سریع باتریها و داغ شدن آنها شوند (خوشبختانه، باتریهای سیب زمینی فقط میتوانند مقدار کمی جریان تأمین کنند، بنابراین اتصال کوتاه در این آزمایش خطرناک نیست).
تصویر ۱ نمودارهای مدار باز، بسته و کوتاه را نشان میدهد.
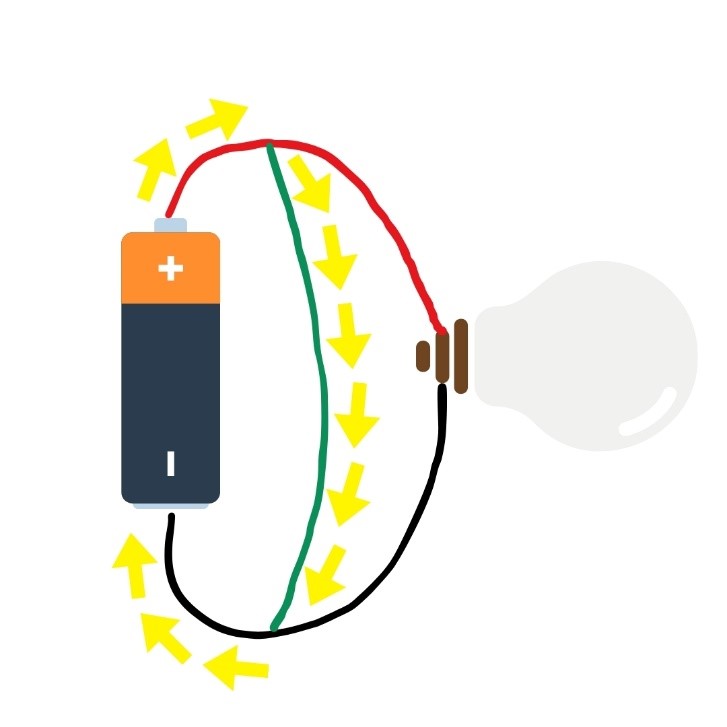
اتصال کوتاه
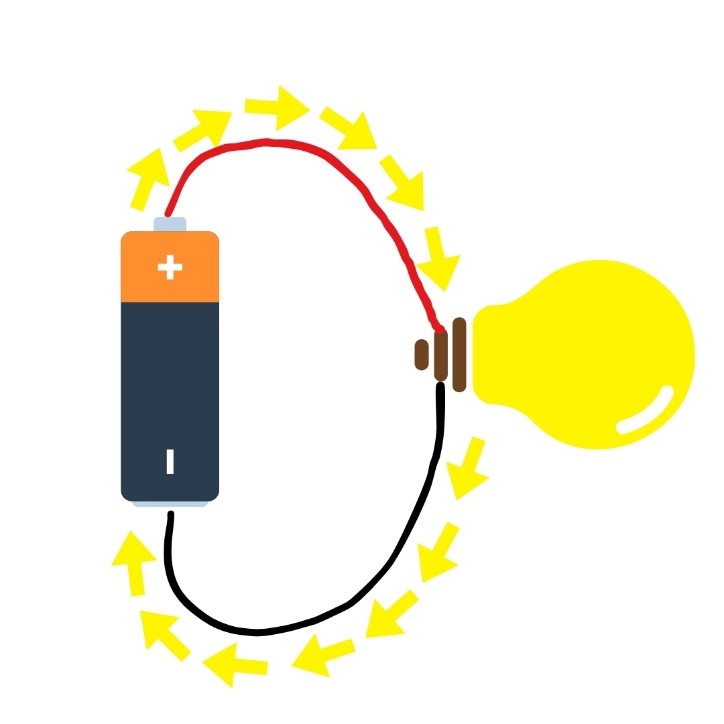
مدار بسته
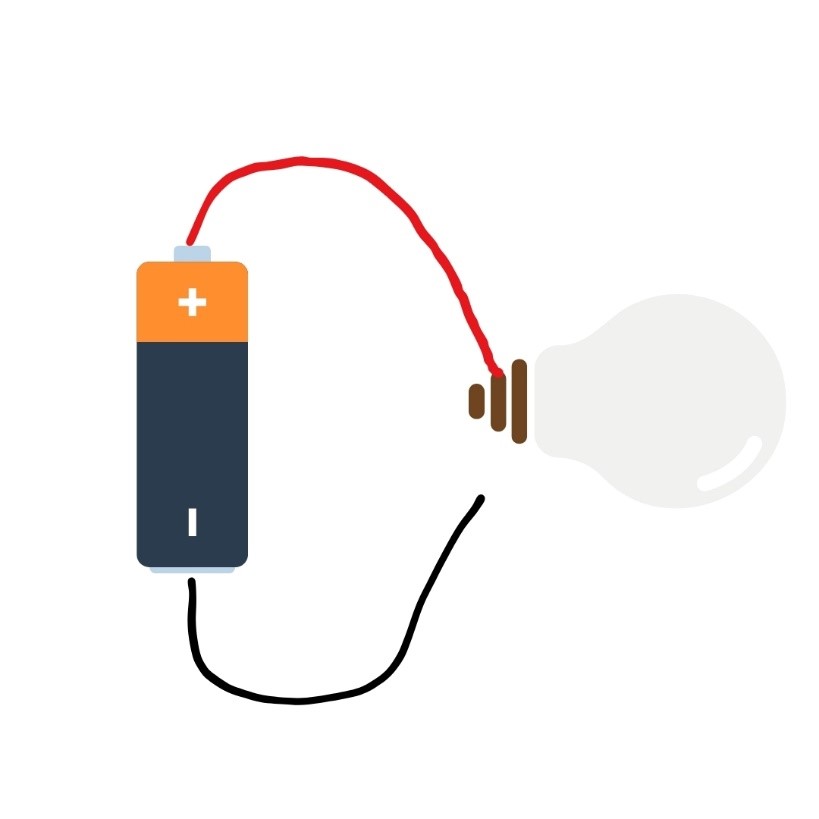
مدار باز
شکل 1. مدارهای بسته، باز و کوتاه. جریان الکتریکی با فلش های زرد نشان داده میشود. در مدار باز، هیچ جریانی به هیچ وجه جریان نمییابد. در مدار بسته، جریان از طریق لامپ عبور میکند و باعث روشن شدن آن میشود. در اتصال کوتاه، جریان مستقیماً بین پایانههای باتری جریان مییابد و لامپ را دور میزند، بنابراین روشن نمیشود.
در مورد مدارهایی که بیش از یک باتری دارند چطور؟ شما احتمالاً از بسیاری از دستگاهها که به دو یا چند باتری نیاز دارند، مانند اسباببازیها یا کنترلهای از راه دور استفاده کردهاید. باتریهای چندگانه میتوانند به دو روش متفاوت متصل شوند: به صورت سری یا موازی. هنگامی که چندین باتری به صورت سری وصل می شوند، پایانه مثبت یک باتری به پایانه منفی باتری بعدی متصل می شود (و اگر بیش از دو باتری وجود داشته باشد این کار تکرار می شود). وقتی باتریها به صورت موازی متصل میشوند، تمام پایانههای مثبت باتریها به هم متصل میشوند و تمام پایانههای منفی باتریها نیز به هم متصل میشوند. این دو پیکربندی در شکل ۲ نشان داده شده است.
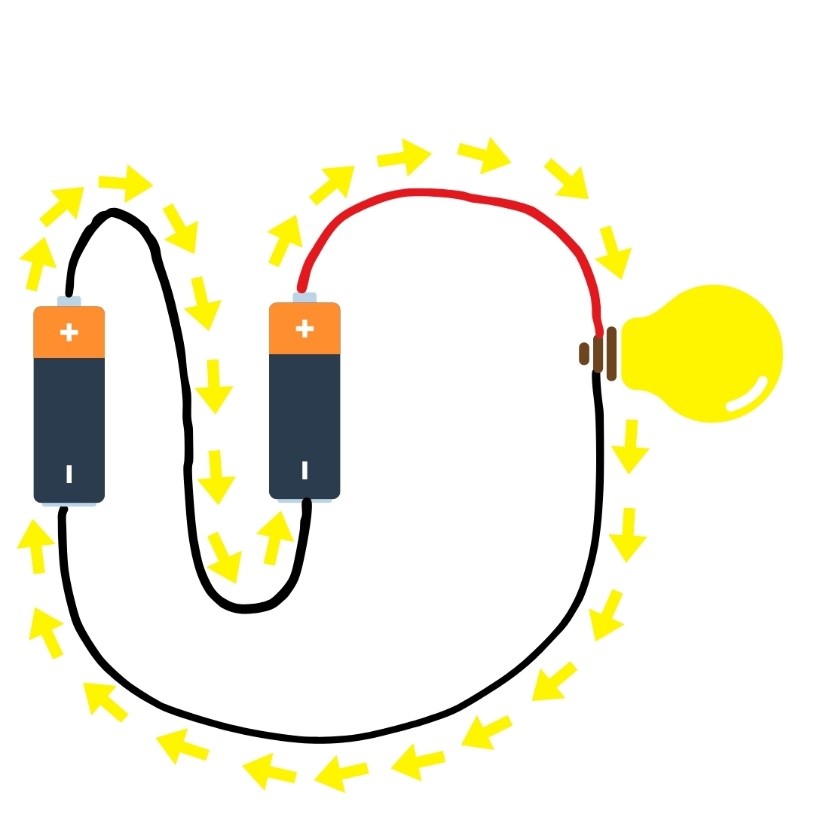
سری
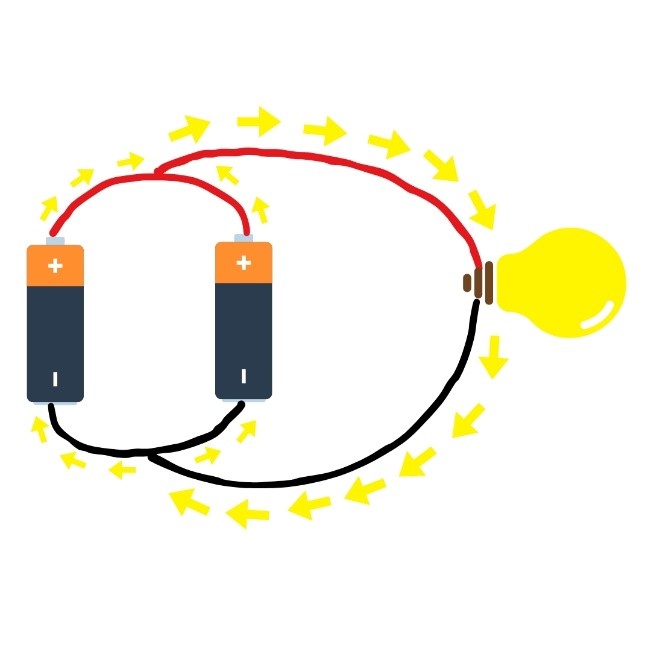
موازی
تصویر 2. باتریهای متصل به صورت سری و موازی. جریان الکتریکی با فلشهای زرد نشان داده میشود.
چرا کسی یک روش را به جای دیگری انتخاب میکند؟ میزان ولتاژ و جریانی که میتوان توسط چندین باتری تامین کرد بسته به اینکه آنها را به صورت سری یا موازی وصل کنید، تغییر میکند و برخی از دستگاههای الکترونیکی ممکن است به میزان معینی از ولتاژ یا جریان نیاز داشته باشند. به عنوان مثال، آیا تا به حال متوجه شدهاید که یک دستگاه کوچک مانند کنترل تلویزیون یا ماوس کامپیوتر ممکن است فقط به دو باتری AAA (نیمقلمی) نیاز داشته باشد، اما یک اسباببازی بزرگتر یا چراغ قوه ممکن است به چهار یا بیشتر باتری AA (قلمی) نیاز داشته باشد؟ این به این دلیل است که هر دستگاه نیازهای الکتریکی متفاوتی برای کارکرد مناسب دارد.
شما میتوانید با تعیین ولتاژ مدار باز و جریان اتصال کوتاه باتریها، میزان ولتاژ یا جریانی را که تعداد معینی از باتر ها میتوانند ارائه دهند اندازهگیری کنید.
ولتاژ مدار باز باتری ولتاژی است که در سر پایانههای یک باتری زمانی که به چیزی وصل نیست، اندازهگیری میشود. این بالاترین ولتاژی است که یک باتری میتواند تامین کند (وقتی باتری به بار متصل می شود ولتاژ کمی کاهش می یابد).
جریان اتصال کوتاه جریانی است که پایانههای باتری به هم متصل میشوند. این بالاترین جریانی است که باتری میتواند تامین کند (هنگامی که باتری به یک بار متصل شود، جریان نیز کاهش مییابد).
وقتی باتریهای شما (سیب زمینی) به صورت سری یا موازی پیکربندی میشوند، ولتاژ و جریان دقیقاً چگونه تغییر میکند؟ در این پروژه از یک مولتی متر، دستگاهی که میتواند مدارهای الکتریکی را اندازه گیری کند، استفاده میکنید.
نکات فنی: شیمی باتری
در باتری، انرژی شیمیایی به انرژی الکتریکی تبدیل میشود. به طور کلی، جریان الکتریکی از جریان الکترونها تشکیل شده است که ذرات باردار منفی هستند. در باتری سیب زمینی، انرژی الکتریکی توسط دو واکنش شیمیایی که در الکترودها اتفاق میافتد (نوارهای فلزی مس و روی) تولید میشود. از آنجایی که مس الکترونگاتیوتر از روی است، تمایل بیشتری به جذب الکترون نسبت به روی دارد. بنابراین، الکترونهای یک باتری سیب زمینی از الکترود روی، آند، به الکترود مس، کاتد، جریان مییابد. اما این الکترونها از کجا میآیند؟ الکترونها از فلز روی مشتق میشوند. هنگامی که روی با الکترولیت در تماس است، واکنش اکسیداسیون زیر رخ میدهد که منجر به آزاد شدن الکترون میشود:
معادله۱ (الکترود روی):
–Zn → Zn2+ + 2e
در حالی که روی به عنوان یک یون مثبت (Zn2+) به الکترولیت میپیوندد، الکترونها از طریق سیمی که الکترودها را به هم متصل میکند جریان مییابند (شکل 3 یک LED متصل به الکترودها را نشان میدهد اما همانطور که در این روش خواهید دید، این میتواند یک مولتی متر نیز باشد. یا یک زنگ).
در اینجا، اتمهای هیدروژن با بار مثبت یا پروتونها (H+)، که از اسیدهای داخل سیبزمینی (اسید فسفریک و اسیدهای آلی) منشأ میگیرند، با جذب بار منفی که توسط الکترونهای اضافی در الکترود مسی ایجاد میشود، جمع میشوند. این پروتونها الکترونهای الکترود مس را طی یک واکنش احیایی میگیرند و به اتمهای هیدروژن خنثی تبدیل میشوند و متعاقباً گاز هیدروژن (H2) را تشکیل میدهند که ممکن است بهعنوان حبابهایی در اطراف الکترود مس مشاهده کنید:
معادله۲ (الکترود مس):
2H+ + 2e− → H2
معادله 3 (واکنش خالص):
Zn + 2H+ → Zn2+ + H2
(گاز هیدروژن و برق)
توجه داشته باشید که خود سیب زمینی تنها منبع انرژی باتری نیست، بلکه به عنوان یک الکترولیت عمل می کند تا انتقال یونهای مربوطه، مانند کاتیونهای روی و پروتونهای اسیدهای آلی و اسید فسفریک موجود در داخل سیب زمینی را تسهیل کند.
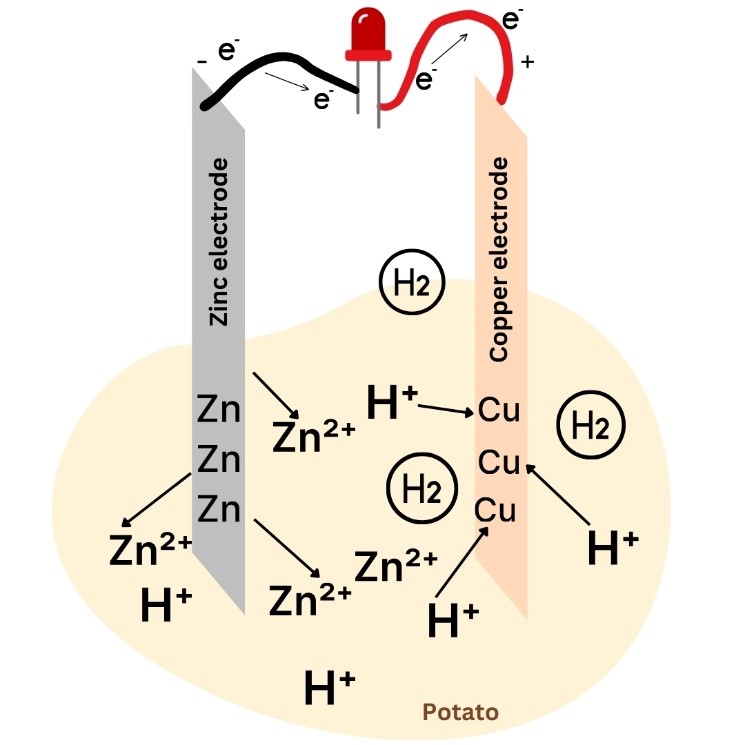
تصویر 3. نمودار واکنش شیمیایی که در باتری سیب زمینی رخ میدهد، با یک LED متصل بین الکترودها. توجه داشته باشید که فلشهایی که حرکت الکترون را در این شکل نشان میدهند در جهت مخالف آنهایی هستند که جریان الکتریکی را در شکلهای 1-2 نشان میدهند.
شما به این موارد از کیت نیاز خواهید داشت:
الکترود مس (3)
الکترود روی (3)
سوسماری (6)
مولتی متر دیجیتال با سیم های تست
زنگ پیزوالکتریک
دیود ساطع کننده نور قرمز (LED) (3)
شما همچنین باید این موارد را که در کیت موجود نیستند جمع آوری کنید:
سیب زمینی (3)، هر نوع درشتی. مطمئن شوید که سیب زمینی هایتان تازه هستند. سیب زمینیهای کهنه و خشک شده به خوبی کار نمیکنند.
خط کش
حوله کاغذی برای تمیز کردن سیب زمینیها
دفترچه یادداشت آزمایشگاهی
امینبیک کیت باتری سیبزمینی را برای استفاده آسان در اختیار شما قرار میدهد
تهیه و تنظیم از:
- مهسا سبزی خباز